Soal Perkembangan Model Atom – Halo adik-adik, kali ini mimin dinas.id akan memberikan rekomendasi kumpulan contoh soal-soal Kimia kelas 10, X KD 3.2 SMA untuk UAS, UTS semester genap, ganjil, gasal. Tentunya, sesuai kisi-kisi pertanyaan tentang perkembangan model atom.
Rangkuman Materi Perkembangan Model Atom
Untuk memudahkan mengerjakan latihan, silahkan pahami ringkasan materi di bawah ini:
Secara singkat Perkembangan model atom dapat dituliskan sebagai berikut:
- Dalton menyarankan bahwa atom adalah bagian terkecil dari materi yang tidak bisa dibagi-bagi lagi.
- Thomson menyatakan bahwa atom adalah partikel positif dengan elektron yang tersebar di dalamnya.
- Rutherford menyatakan bahwa atom terdiri dari inti atom yang bermuatan positif dan dikelilingi elektron yang bermuatan negatif.
- Neils Bohr menyarankan bahwa elektron yang berputar mengelilingi atom berada pada lintasan atau tingkat energi tertentu.
- Mekanika Kuantum menemukan daerah kebolehjadian ditemukannya elektron yang dinamakan dengan orbital.
Soal Pilihan Ganda
Oke, bacalah petunjuk di bawah ini sebelum menjawab soal!
Berikan jawaban yang paling benar!
1. Gambar berikut ini merupakan perkembangan model atom.
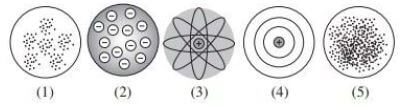
Model atom Rutherford adalah model atom nomor ….
A. (1)
B. (2)
C. (3)
D. (4)
E. (5)
2. Teori atom yang dapat menerangkan adanya spektrum atom hidrogen adalah teori atom ….
A. Bohr
B. Rutherford
C. Thomson
D. Rydberg
E. Dalton
3. Pokok teori atom Thomson dititik beratkan pada ….
A. Atom terdiri dari elektron – electron
B. Elektron sebagai penyusun utama atom
C. Atom sebagai bola masif yang hanya berisi electron
D. Atom sebagai bola masif bermuatan positif yang di dalamnya tersebar elektron sehingga keseluruhannya bersifat netral
E. proton dan elektron adalah bagian penyusun atom yang keduanya saling Meniadakan
4. Perhatikan beberapa pernyataan berikut!
(1) Hanya mampu menjelaskan sepektrum atom hydrogen
(2) Tidak mampu menjelaskan sepektrum atom-atom berelektron banyak
(3) Tidak dapat menerangkan alasan elektron tidak jatuh ke dalam inti
(4) Bertentangan dengan teori gelombang elektromagnetik Maxwell
(5) Jarak elektron dengan inti terlalu jauh sehingga tidak ada gaya sentripetal
Kelemahan teori atom Rutherford ditunjukkan oleh angka….
A. (1) dan (2)
B. (1 )dan (3)
C. (2) dan (5)
D. (3) dan (4)
E. (4) dan (5)
5. Dibandingkan dengan teori atom Rutherford, teori atom Niels Bohr mempunyai kelebihan dalam hal…
A. Jumlah proton dan jumlah elektron
B. Massa atom yang terpusat pada inti atom
C. Muatan proton yang sama dengan muatan elektron
D. Keberadaan elektron pada tingkat-tingkat energi tertentu saat mengelilingi inti atom
E. Keberadaan proton dan neutron dalam inti atom serta electron mengelilingi inti atom
6. Elektron-elektron dalam atom beredar mengelilingi inti dan berada pada lintasan (tingkat energi) tertentu. Elektron dapat berpindah dari satu tingkat energi ke tingkat energi lainnya disertai penyerapan atau pelepasan energi. Pernyataan ini dikemukaan oleh …
A. Dalton
B. Thomson
C. Rutherford
D. Niels Bohr
E. Schrodinger
7. Kulit-kulit atom bukan merupakan kedudukan yang pasti dari suatu elektron, melainkan hanya suatu kebolehjadian ditemukannya elektron. Pernyataan ini dikemukakan oleh ….
A. Wernerg Heisenberg
B. Niels Bohr
E. Ernest Rutherford
D. J.J Thomson
E. Goldstein
8. Elektron dapat berpindah dari suatu lintasan ke lintasan yang lain sambil menyerap atau memancarkan energi. Teori yang merupakan penyempurnaan dari teori atom Rutherford ini dinamakan teori ….
A. Niels Bohr
B. Dalton
C. Thomson
D. Rutherford
E. Mekanika Kuantum
Kunci Jawaban dan Pembahasan
1. C → Pembahasan: Menurut Rutherford, atom terdiri atas inti atom yang bermuatan positif dikelilingi oleh elektron yang bermuatan negative.
2. A → Pembahasan: Sudah jelas.
3. D → Pembahasan: Teori Atom Thomson: Atom adalah partikel positif dengan elektron –elektron yang tersebar didalamnya.
4. D → Pembahasan:
Kelemahan teori atom Rutherford:
- Tidak dapat menjelaskan penyebab elektron tidak jatuh ke dalam inti atom. Hal ini bertentangan dengan teori gelombang elektromagnetik Maxwell. Karena berdasarkan teori gelombang elektromagnetik Maxwell, gerakan elektron mengitari inti disentari dengan pemancaran energi, hal tersebut akan menyebabkan berkurangnya elektron dan lintasannya semakin mendekati inti, lalu jatuh ke dalam inti atom.
- Tidak dapat menjelaskan terjadinya sepektrum garis pada atom hidrogen.
5. D → Pembahasan: Menurut Bohr, elektron mengelilingi inti atom pada tingkat energi tertentu. Ketika elektron berpindah ke tingkat energi yang lebih tinggi maka elektron akan menyerap energi, dan sebaliknya ketika elektron berpindah ke tingkat energi yang lebih rendah maka elektron akan memancarkan energi.
6. D → Pembahasan:
Niels Bohr mengemukakan bahwa:
- Atom terdiri atas inti atom yang bermuatan positif dan dikelilingi oleh elektron yang bermuatan negatif di dalam suatu lintasan.
- Elektron dapat berpindah dari satu lintasan ke lintasan yang lain dengan menyerap atau memancarkan energi sehingga energi elektron atom itu tidak akan berkurang. Jika berpindah dari lintasan rendah ke lintasan yang lebih tinggi maka elektron akan menyerap energi. Sebaliknya, jika berpindah dari lintasan tinggi ke rendah maka akan memancarkan energi.
7. A → Pembahasan: Teori ketidak pastian Heisenberg menyatakan bahwa “kedudukan dan kecepatan gerak elektron tidak dapat ditentukan secara pasti, yang dapat ditentukan hanyalah kemungkinan terbesar atau probabilitas kebenaran elektron pada jarak tertentu dari inti atom.”
8. A → Pembahasan: Elektron dapat berpindah dari suatu lintasan ke lintasan yang lain sambil menyerap atau memancarkan energi. Teori yang merupakan penyempurnaan dari teori atom Rutherford adalah Teori Atom Niels Bohr.
Demikian prediksi contoh soal dan jawaban UTS, UAS modul kimia Kelas 10, X SMA, dipelajari yah. Merdeka Belajar!









