Dalam topik ini kita akan fokus pada materi pengantar biokimia sebagai awalan mempelajari biokimia. Olehnya, kamu harus membaca artikel ini dan artikel biokimia terkait lainnya.
Sejarah Biokimia
Selama berabad-abad asal mula kehidupan diperdebatkan dan menjadi polemik yang tak kunjung selesai sampai teori Abiogenesis diruntuhkan oleh teori Biogenesis pada tahun 1822-1895 oleh Louis Pasteur.
Pertanyaan berikutnya adalah, jika makhluk hidup berasal dari makhluk hidup, dari manakah asal mula makhluk hidup yang pertama?
Untuk menjawab itu, muncullah teori evolusi kimia oleh Harold Urey, yang menyatakan bahwa pada periode tertentu, atmosfer bumi mengandung molekul metana (CH4), amonia (NH4), air (H2O), dan karbon dioksida (CO2).
Karena pengaruh energi dan sinar kosmis yang luar biasa besarnya, zat-zat tersebut bereaksi menghasilkan suatu zat kehidupan.
Pada perioda berikutnya, percobaan oleh Stanley Miller berhasil membuktikan teori Harold Urey, bahwa unsur dasar kehidupan adalah C, H, O, N seperti yang diketahui sekarang.
Namun tetap saja menyisakan pertanyaan besar, yaitu bagaimana zat ini hidup?
Terlepas dari pertanyaan yang tidak kunjung selesai tersebut, kemajuan teknologi semakin dapat membuktikan zat paling dasar dalam struktur kehidupan dalam bentuk partikel, dan perilaku partikel tersebut terhadap kehidupan.
Berbagai penelitian menunjukkan bahwa partikel-partikel ini berinteraksi satu dengan yang lain, juga terhadap lingkungan dalam membangun dan menjaga kelangsungan kehidupan. Reaksi ini berlangsung begitu komplek hingga sebuah reaksi kadang sulit dimengerti prosesnya dan manfaat hasil akhirnya.
Atom Sebagai Substansi Dasar Kehidupan
Untuk memperdalam khasanah biokimia kamu, lanjut bahas tentang struktur paling dasar penyusun kehidupan dan reaktan proses kimia dalam kehidupan adalah atom. Atom merupakan partikel terkecil dari sebuah elemen yang tersusun atas neutrons (tidak bermuatan), proton (bermuatan positif) dan elektron (bermuatan negatif).
Elemen merupakan bagian paling sederhana dari sebuah materi. Sebagai contoh Karbon (C) atau Hidrogen (H), masing-masing merupakan sebuah elemen.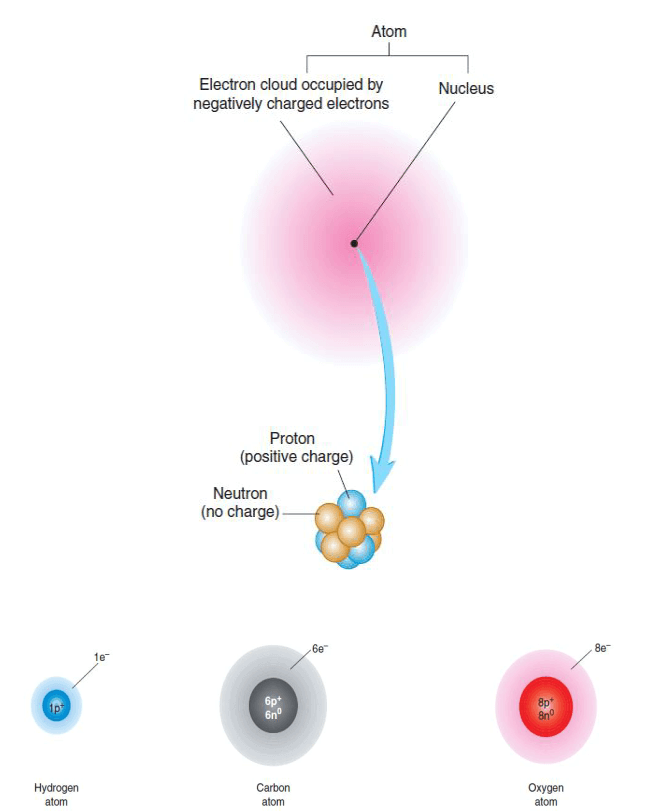
Sampai saat ini baru diketahui ada 112 elemen penyusun struktur kehidupan seperti dapat dibaca pada gambar 1.2. Elemen tersebut akan membentuk materi.
Pengertian secara umum yang dimaksud materi adalah segala sesuatu yang menempati ruang dan memiliki masa. Materi dibedakan menjadi tiga golongan, yaitu materi padat, cari dan gas.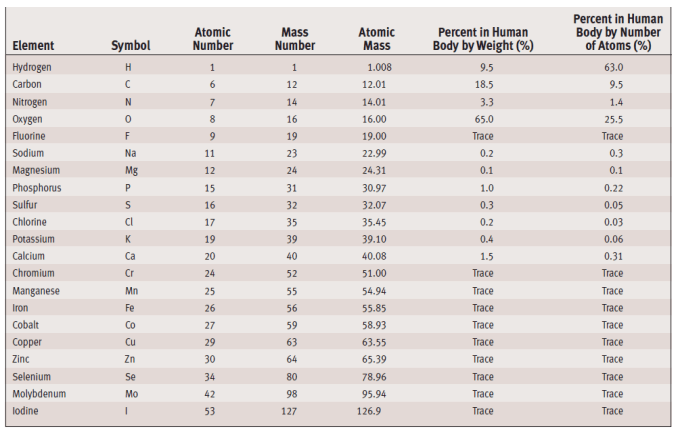
Materi padat, tersusun atas molekul-malekul yang berikatan sangat kuat atau dengan kata lain gaya tarik antar molekul sangat kuat sehingga sulit untuk dipisahkan. Dengan demikian materi padat memiliki karakter sebagai berikut:
- Memiliki bentuk yang relatif tetap.
- Strukturnya relatif stabil terhadap paparan lingkungan.
- Wujud sulit diubah kecuali dihancurkan.
- Contoh materi jenis ini pada mahluk hidup adalah: tulang, otot, lemak, sel darah merah, pembuluh darah, rambut, dan lain-lain.
Materi cair, molekul penyusun materi cair berikatan lebih longgar dan mudah dipisahkan. Materi cair memiliki karakter sebagai berikut:
- Bentuk berubah-ubah menurut tempatnya.
- Strukturnya dapat berikatan dengan struktur yang lain bahkan dapat membentuk struktur baru dengan sifat dan karakter yang sama sekali berbeda dengan struktur awalnya.
- Mudah terpengaruh lingkungan dan berubah wujud.
- Contoh materi cair adalah: plasma, thrombosit, lekosit, cairan limphe, liquorcerebrospinal, cairan interartikular, dan sebagainya.
Materi gas, tersusun dari molekul yang berikatan dengan sangat longgar, serta memiliki karakter sebagai berikut:
- Mudah dipengaruhi oleh lingkungan (suhu, tekanan, ketinggian dan lain-lain).
- Keberadaannya dapat berasal dari alam atau sebagai hasil suatu reaksi materi yang lain.
- Reaktif terhadap materi yang lain untuk membentuk materi baru dengan sifat dan karakter yang berbeda pula.
- Sangat mempengaruhi kelangsungan kehidupan.
- Contoh: oksigen (o2), karbonmonoksida (co), karbondiaoksida (co2), ozon (o3), dan sebagainya.
Cara atom-atom materi itu bereaksi membentuk makhluk hidup dapat dipelajari pada gambar di bawah ini: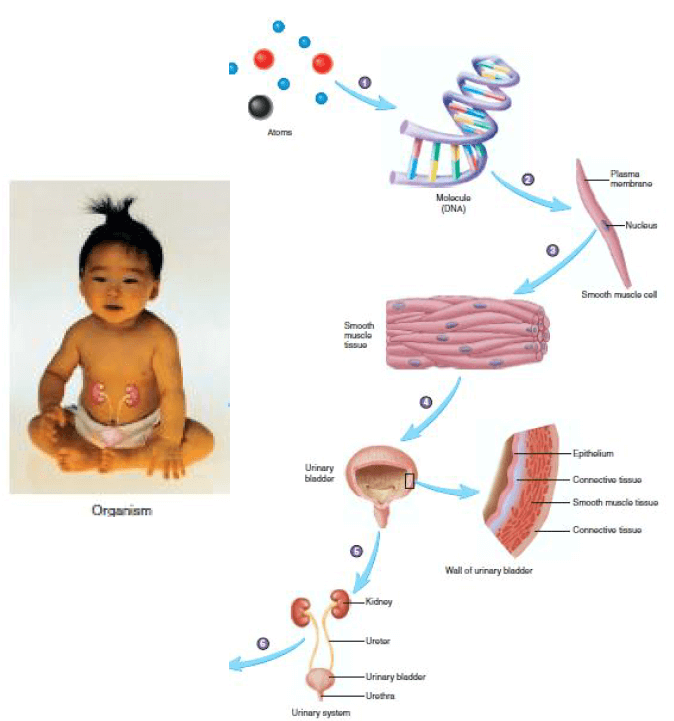
Interaksi Atom Dalam Membangun Sistem Kehidupan
Lanjutan pengantar biokimia, fokus yah!
Partikel-partikel atom yang ada dalam tubuh secara terus menerus berinteraksi satu dengan yang lain dan menghasilkan suatu produk yang dibutuhkan untuk menunjang sistem kehidupan melalui berbagai jenis reaksi.
Reaksi-reaksi ini terjadi karena molekul-molekul mengalami ikatan kimia, berikatan sesuai dengan kemampuan melepas atau menarik unsur yang lain dan membentuk suatu produk yang baru.
Ikatan kimia dapat terjadi antar molekul karena peran elektron-elektron yang berada di lintasan paling luar, yaitu dengan cara melepas elektron untuk berpindah ke molekul yang lain, atau menerima elektron dari molekul yang lain, atau memakai bersama elektron untuk membentuk ikatan. Proses Ini merupakan prinsip pembentukan ikatan kimia molekul untuk menjadi substrat yang lain atau ketika terjadi proses penguraian (disosiasi).
Ada dua model ikatan utama yaitu ikatan ion tunggal dan ikatan kovalen.
1. Ikatan Ion Tunggal (Ionic Bonding)
Sebuah atom bermuatan netral karena ada keseimbangan antara jumlah proton dan elektron. Jika sebuah atom kehilangan atau menerima elektron, maka akan terjadi perubahan keseimbangan proton elektron dan terbentuk sebuah partikel yang disebut ion.
Setelah atom kehilangan elektron, maka jumlah proton akan lebih banyak dari elektron, sehingga partikel atom ini memiliki muatan positif. Atom sodium (Na) dapat kehilangan elektron sehingga muatannya menjadi positif, seperti tampak pada gambar di bawah ini.
Atom Chlorida (Cl) dapat menerima elektron dan akan menjadi on yang bermuatan negatif (Cl-). Atom bermuatan positif disebut sebagai kation, dan yang bermuatan negatif disebut anion.
Karena muatan yang berlawanan saling menarik, maka ion dan kation akan berikatan yang di sebut sebagai ikatan ionik. Contohnya Sodium dan Chloride bereaksi melalui ikatan ionik membentuk sodium chloride (NaCl) atau lebih dikenal sebagai garam dapur seperti pada gambar di bawah ini.
2. Ikatan Kovalen (Covalent Bonding)
Ikatan kovalen terjadi ketika atom memakai bersama satu atau lebih elektron, untuk bergabung sebagai molekul. Contoh ikatan kovalen adalah ikatan antara dua atom hidrogen membentuk molekul hidrogen (H2), yang lebih stabil daripada atom hidrogen, karena mengikuti konfigurasi gas mulia Helium (He), yang memiliki 2 elektron. Dua atom hidrogen sekarang menyatu dalam ikatan kovalen.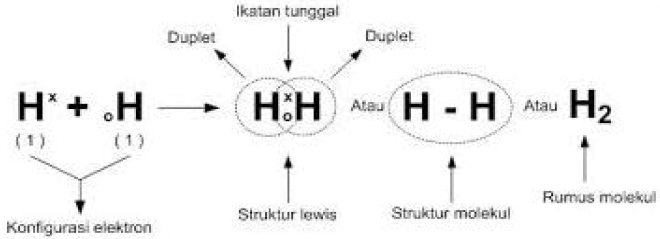
Jika sepasang elektron dibagi di antara dua atom maka dihasilkan ikatan kovalent tunggal seperti pada H2 dan H2O.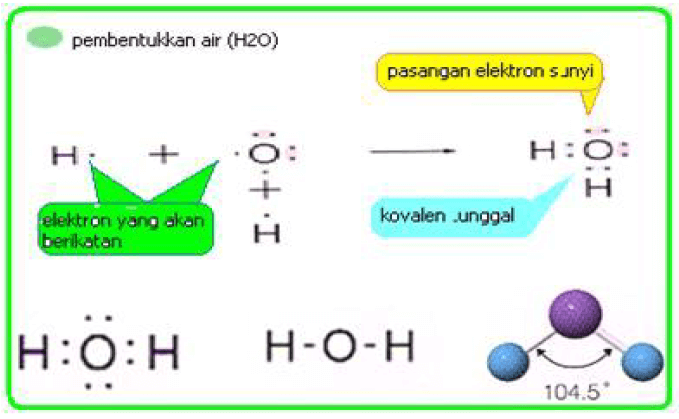
Ikatan ini dituliskankan dengan garis tunggal diantara simbol atom yang berikatan (contoh: H2, H—H atau H2O, H─O─H).
Jika dua atom memakai bersama empat elektron, yaitu dua dari masing-masing atom, akan menghasilkan ikatan kovalen rangkap dua, misalnya atom karbon dengan dua atom oksigen akan menghasilkan karbodioksida maka terjadi dua ikatan kovalen rangkap 2.
Ikatan ini di tulis dengan garis rangkap di antara atom yag berikatan (O═C═O). Keterangan mengenai mekanisme pembentukan ikatan ionik dan kovalen, telah dibahas dalam mata kuliah Kimia Dasar, terutama topik tentang Ikatan Kimia dan Susunan Berkala.
Alangkah baiknya Anda membaca kembali materi Kimia Dasar ini!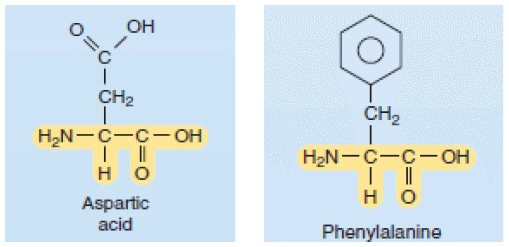
Pada reaksi kimia atom, ion, molekul atau campuran saling berinteraksi membentuk atau memutus rantai ikatan kimia. Semua zat yang terlibat dalam suatu reaksi kimia disebut sebagai reaktan dan zat yang dihasilkan dari reaksi kimia disebut sebagai produk.
Ada tiga hal yang dapat terjadi dari suatu reaksi kimia. Pertama bahwa dalam beberapa reaksi hanya sedikit reaktan yang dicampurkan untuk menghasilkan produk yang lebih komplek misalnya untuk mensintesa molekul yang komplek pada tubuh dari asupan gizi (nutrient) yang didapat dari makanan.
Kedua adalah reaksi yang menguraikan dari molekul komplek menjadi produk yang lebih sederhana. Contohnya pemecahan makanan menjadi produk dasar yang lebih sederhana. Ketiga Ikatan atom yang membentuk produk baru atau memecah atau memutus ikatan lain.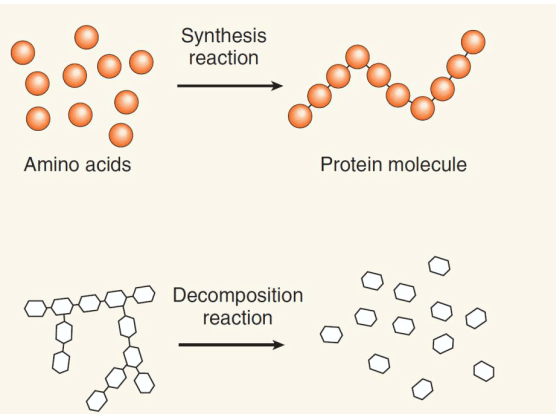
Reaksi Pembentukan
Jika dua reaktan atau lebih dicampurkan dan membentuk produk baru yang lebih besar maka proses ini disebut sebagai reaksi pembentukan (reaksi sintesis). Sebagai contoh, gabungan dua asam amino membentuk dipeptida, suatu reaksi sintesis yang melepaskan air dari ikatan asam amino, dan reaksi yang menghasilkan air ini disebut sebagai dehydration reaction atau reaksi dehidrasi. Jika reaksi tersebut menghasilkan produk lain dengan mengurai reaktan, maka disebut reaksi dekomposisi, seperti tampak pada gambar 1.9.
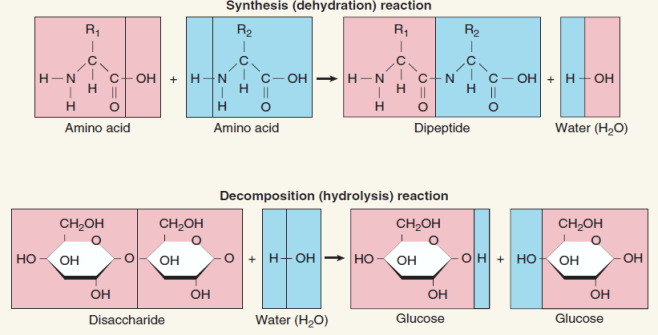
Model Struktur Molekul Yang Terbentuk dari Ikatan Kimia Dalam Jaringan Tubuh Manusia
Wujud molekul dengan struktur kimia tertentu dalam jaringan tubuh yang mudah dan sering dikenal dalam keseharian adalah dalam bentuk sebagai berikut.
1. Karbohidrat
Disebut sebagai karbohidrat karena tulang punggung ikatan kimia ini adalah rantai karbon yang berkombinasi dengan Oksigen dan Hidrogen yang membentuk air (hydrated).
Karbohidrat memiliki rangkaian yang bervariasi mulai dari yang sederhana (monosaccharides) sampai yang paling komplek (polysaccharides). Molekul ini merupakan bahan utama energi untuk kehidupan.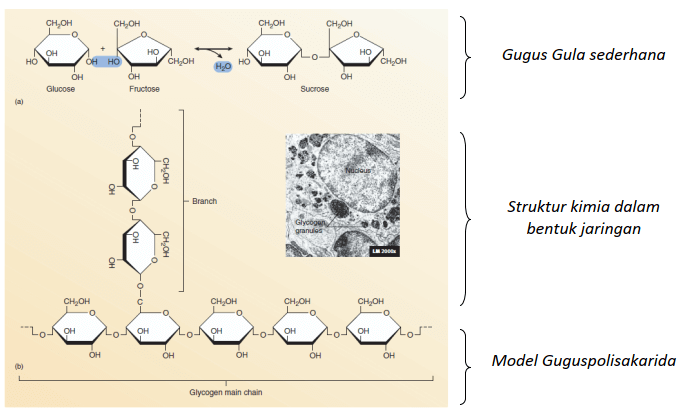
2. Lemak
Struktur kimia lemak mirip dengan karbohidrat tetapi masih ditambah ikatan dengan fosfor dan nitrogen. Sama dengan karbohidrat bahwa lemak juga mempunyai varian lain sesuai dengan panjang rantai dan ikatan dengan elemen yang lain. Dalam tubuh lemak memiliki fungsi yang fisiologik terhadap organ lain dan sebagai cadangan energi untuk dipecah sebagai karbohidrat.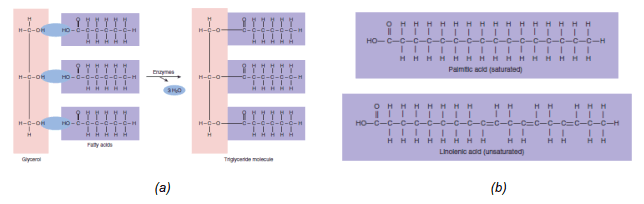
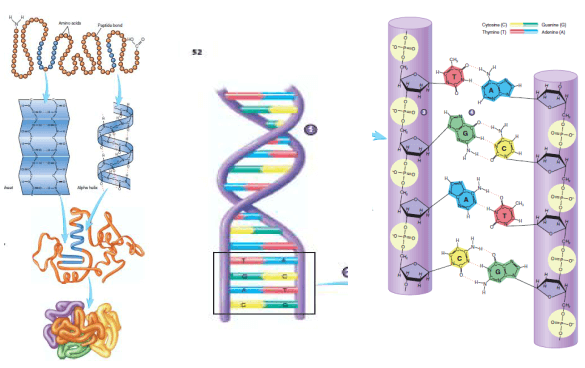
3. Protein
Seluruh gugus rantai protein memiliki atom karbon, hidrogen, oksigen, nitrogen dan juga ada yang mengandung sulfur (belerang) yang tersusun dalam ikatan kovalen, dan pada kondisi yang lain, rantai protein juga mengikat besi (ferum) dan Iod. Dalam tubuh protein memiliki peran yang sangat penting untuk seluruh proses kelangsungan hidup. Sama dengan karbohidrat dan lemak, protein juga memiliki struktur dari yang paling sederhana sampai yang paling komplek.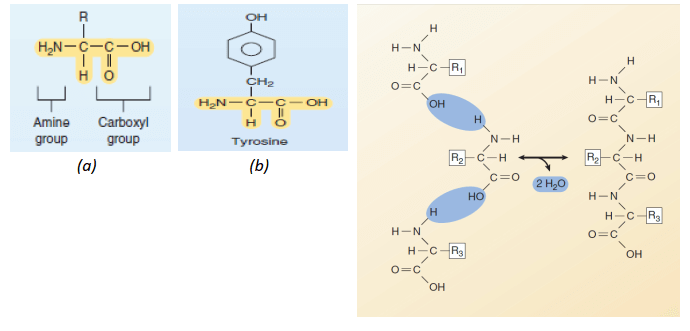
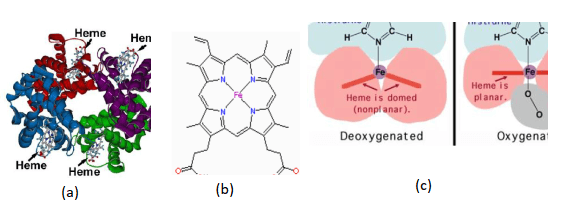
Demikian penjelasan seputar pengantar materi biokimia, semoga bermanfaat untuk memahamkan kita tentang biokimia!









